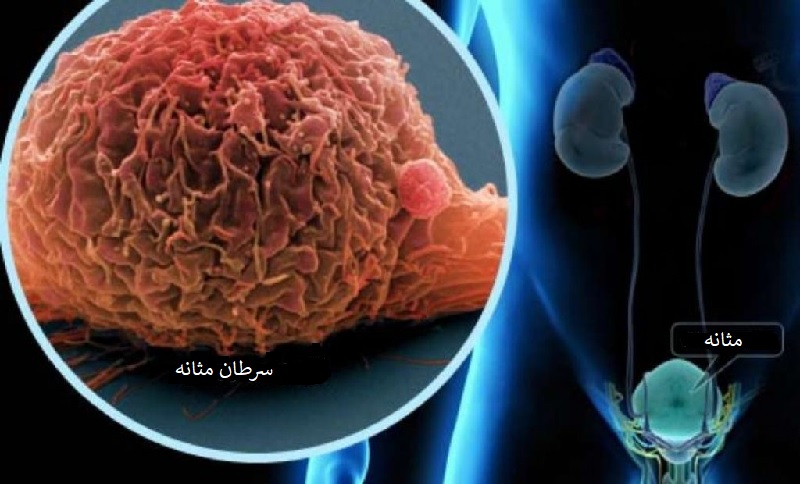
درمان سرطان مثانه با داروی اپدیوو و تایید سازمان غذا دارو آمریکا FDA
سازمان غذا و داروی ایالات متحده (FDA) داروی اوپدیوو (نیوولوماب) ، را برای درمان بیماران مبتلا به سرطان یوروتلیال در مراحل اولیه پرخطر و به صورت موضعی پیشرفته یا متاستاتیکی که بیماری آنها تا یک سال پس از شیمی درمانی حاوی پلاتینیوم پیشرفت کرده است، تأیید نموده. از آنجایی که آزمایشهای بالینی تاییدی نشان دادهاند که اوپدیوو عود بیماری را به تاخیر انداخته و نتایج را در صورت استفاده در مراحل اولیه بیماری و در شرایط کمکی بهبود میبخشد.
بازدارنده ها در نقطه بازرسیPD-1 اوپدیوو، بقای شخص را پس از برداشتن سرطان مثانه از طریق جراحی بهبود می بخشد.
سرطان مثانه تنها در سال جاری در حدود ۷۷۰۰۰ نفر در ایالات متحده تشخیص داده می شود. میانگین سنی که بیماران مبتلا به سرطان مثانه تشخیص داده می شوند ۷۰ سال است که ۸۰ درصد از این بیماران قبلاً سیگاری بوده اند. شایع ترین نوع سرطان مثانه، کارسینوم یوروتلیال است که به موجب آن سرطان در سلول های پوشاننده مثانه شروع می شود.
درباره اوپدیوو (نیوولوماب)
اوپدیوو نوعی ایمونوتراپی به نام بازدارنده چک پوینت است که با آزاد کردن نقاط بازرسی که سرطان برای خاموش کردن سیستم ایمنی از آن استفاده میکند، به بازیابی سیستم ایمنی بدن در مبارزه با سرطان کمک میکند. PD-1 و PD-L1 پروتئین هایی هستند که انواع خاصی از پاسخ های ایمنی را مهار می کنند و به سلول های سرطانی اجازه می دهند از حمله سلول های ایمنی بدن فرار کنند. داروهای مهارکننده ایست بازرسی که مسیر PD-1 را مسدود می کنند، توانایی سیستم ایمنی را برای مبارزه با سرطان افزایش می دهند. این داروها با مسدود کردن اتصال لیگاند PD-L1، توانایی سلول های ایمنی را برای شناسایی و مبارزه با سلول های سرطانی ریه بازیابی می کنند.
اوپدیوو بقای بدون بیماری را در سرطان یوروتلیال پرخطر دو برابر می کند
درمان با اوپدیوو® (نیوولوماب) پس از جراحی با یا بدون شیمی درمانی مبتنی بر سیس پلاتین، بقای بدون بیماری را در بیماران مبتلا به سرطان یوروتلیال مهاجم عضلانی بهبود می بخشد.
درباره کارآزمایی بالینی چک میت 274 مرحله III
این کارآزمایی استفاده از اوپدیوو (کمکی) پس از جراحی را در ۷۰۹ بیمار مبتلا به سرطان یوروتلیال مهاجم عضلانی مثانه، حالب یا لگن کلیه که تحت عمل جراحی رادیکال با یا بدون پیش-جراحی (نئوادجوانت) شیمیدرمانی مبتنی بر سیس پلاتین قرار گرفتند، ارزیابی کرد. بیماران با خطر بالای عود بر اساس مرحله تومور در عمل جراحی با اوپدیوو یا دارونما یک هفته در میان به مدت ۱ سال تحت درمان قرار گرفتند و به طور مستقیم با هم مقایسه شدند.
درمان اوپدیوو به طور قابل توجهی زمان عود سرطان را به تاخیر انداخت. بیماران تحت درمان اوپدیوو به طور متوسط ۲۱ ماه بدون عود سرطان زنده ماندند در حالی که تنها ۱۱ ماه برای افرادی که دارونما دریافت کردند این اتفاق افتاد. سود حاصل از درمان اوپدیوو صرف نظر از وضعیت PD-L1 بود. در بیمارانی که تومورهای آنها بیان PD-L1 1٪ یا بالاتر داشتند، ایمونوتراپی اوپدیوو باعث کاهش ۴۵٪ در خطر عود بیماری یا مرگ شد.
درمان کلی به خوبی تحمل شد و شایع ترین عوارض جانبی مرتبط با درمان اسهال، کولیت و پنومونیت بود.
اوپدیوو اولین درمان ایمنی است که در شرایط کمکی مورد استفاده قرار می گیرد که از نظر بالینی بهبود معنی داری در بقای عاری از بیماری برای بیماران مبتلا به سرطان یوروتلیال مهاجم عضلانی پرخطر پس از جراحی رادیکال با هدف درمانی ایجاد می کند. این کارآزمایی منجر به تایید FDA اوپدیوو برای استفاده به عنوان درمان کمکی بیماران مبتلا به سرطان یوروتلیال شد که در معرض خطر بالای عود سرطان پس از انجام جراحی برداشتن سرطان خود در آگوست ۲۰۲۱ هستند.
تایید در بیماری پیشرفته
اوپدیوو ، که یک مهارکننده گیرنده مرگ سلولی برنامه ریزی شده است، دومین ایمونوتراپی تایید شده برای درمان سرطان پیشرفته مثانه بود. FDA همچنین تسنتریک(آتزولیزوماب) را که به عنوان یک مهارکننده مرگ سلولی برنامه ریزی شده لیگاند-۱ عمل می کند، در می ۲۰۱۶ تایید نمود.
این تایید بر اساس مطالعه ای بر روی ۲۷۰ بیمار مبتلا به سرطان یوروتلیال موضعی پیشرفته یا متاستاتیک بود که پیشرفت بیماری را در طول یا بعد از شیمی درمانی حاوی پلاتینیوم تجربه کردند، یا بیماری آنها طی ۱۲ ماه پس از درمان نئوادجوانت یا ادجوانت با شیمی درمانی حاوی پلاتینیوم پیشرفت کرد.
نرخ پاسخ عینی پس از درمان اوپدیوو 19.6٪ بود. ۷ بیمار پاسخ کامل و ۴۶ نفر پاسخ نسبی داشتند. میانگین مدت پاسخ تخمین زده شده ۱۰.۳ ماه بود. FDA خاطرنشان می کند که برخی از پاسخ ها پس از قطع داده ها ادامه داشت.
این متن توسط تیم محتوا و ترجمه وبسایت سامانه جامع سلامت سین سا گردآوری شده است.